Les cytokines sont un terme général désignant une classe de polypeptides ou de glycoprotéines à petites molécules ayant une activité biologique étendue, synthétisées et sécrétées par des cellules immunitaires ou certaines cellules non immunitaires, qui ont pour fonction de réguler la fonction immunitaire de l'organisme, de médier les réponses inflammatoires et de participer à la réparation des tissus. et favorisant la cicatrisation des plaies. Dans le développement des maladies tumorales, les cytokines sont étroitement liées au statut immunitaire, à la progression de la maladie et au pronostic des patients.
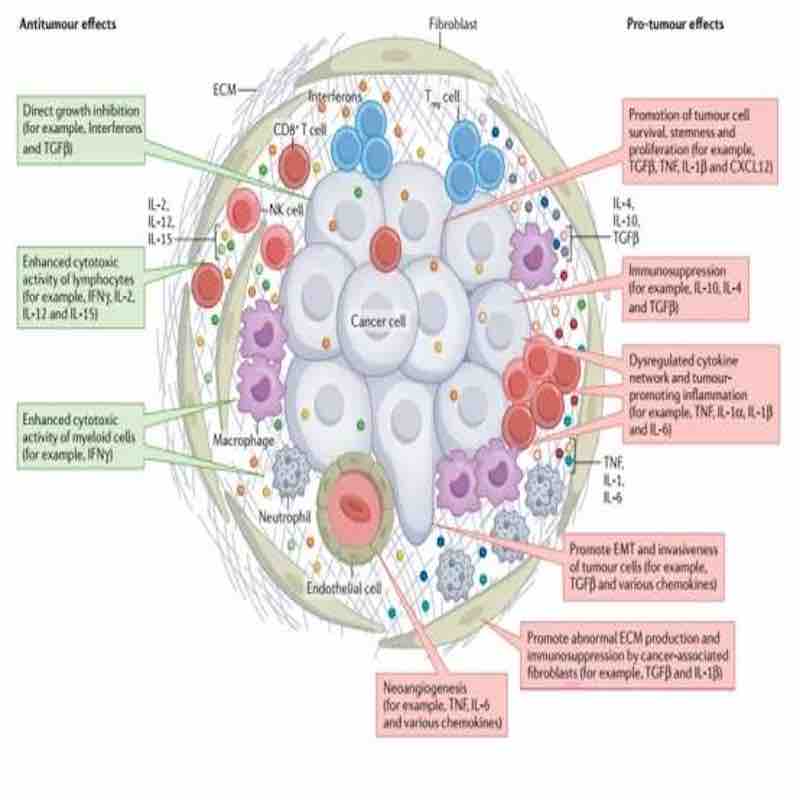
Les cytokines jouent un rôle essentiel dans le microenvironnement tumoral et servent de ponts entre les cellules pour communiquer entre elles. Certaines cytokines sont capables de renforcer la réponse de défense naturelle de l'organisme face aux tumeurs, mais en même temps, de nombreuses cytokines peuvent être surproduites ou dysfonctionnelles en cas de cancer. Par conséquent, il existe de solides arguments en faveur de l’utilisation de cytokines et de leurs inhibiteurs dans les stratégies de traitement du cancer afin de moduler ces médiateurs clés et de restaurer leur fonction normale, combattant ainsi plus efficacement les tumeurs.
Application clinique des cytokines dans les tumeurs
Les cytokines sont d'importants médiateurs qui médient les réponses immunitaires des cellules antitumorales et l'immunosuppression tumorale, et la surveillance des niveaux de cytokines devrait couvrir une variété de types impliqués dans différents processus biologiques, y compris les activateurs immunitaires tels que l'IL-2, l'IL-12, l'IFN-γ, etc. ., des facteurs immunosuppresseurs tels que l'IL-10, le TGF-β, l'IL-8, etc., des facteurs pro-tumoraux tels que l'IL-6, l'IL-8 et des facteurs pro-inflammatoires tels que le facteur de nécrose tumorale TNF-α, IL -1β, IL-6, etc.
Application des cytokines à la détection précoce du cancer gastrique
Des études ont montré que l'IL-6 présente la meilleure valeur diagnostique pour distinguer les témoins sains des groupes de cancer gastrique, avec une ASC de 0,92. Lorsque le CEA, le CA724, l’IL-6, l’IL-8 et le TNF-α ont été analysés ensemble, l’ASC différenciant le groupe témoin sain du groupe atteint de cancer gastrique a atteint 0,95. Pour le cancer gastrique précoce et avancé, l’ASC était respectivement de 0,95. La sensibilité diagnostique était de 89,66 %, 84,21 % et 92,31 %, et la spécificité était de 92,42 %, 90,91 % et 90,91 %, respectivement. Un modèle de diagnostic comprenant le CEA, le CA724, l'IL-6, l'IL-8 et le TNF-α a été établi, ce qui pourrait constituer un complément potentiel au dépistage précoce du cancer gastrique.
Population et calendrier de test recommandés
Patients atteints de tumeurs de novo : surveillance avant et après traitement
Patients hospitalisés en oncologie : suivi de base de l’admission
Patients traités par CAR-T/PD-1/PD-L1 : dans les 14 jours suivant le traitement, les patients atteints de tumeurs traités par chimioradiothérapie, anti-infectieux et chirurgical ont été surveillés quotidiennement avant et après le traitement, et les patients sous chimioradiothérapie ont été testés une fois par cours. de traitement
Patients présentant des tumeurs et une inflammation : surveillés une fois par jour
Patients atteints de tumeurs de novo : surveillance avant et après traitement
Patients hospitalisés en oncologie : suivi de base de l’admission
Patients traités par CAR-T/PD-1/PD-L1 : dans les 14 jours suivant le traitement, les patients atteints de tumeurs traités par chimioradiothérapie, anti-infectieux et chirurgical ont été surveillés quotidiennement avant et après le traitement, et les patients sous chimioradiothérapie ont été testés une fois par cours. de traitement
Patients présentant des tumeurs et une inflammation : surveillés une fois par jour
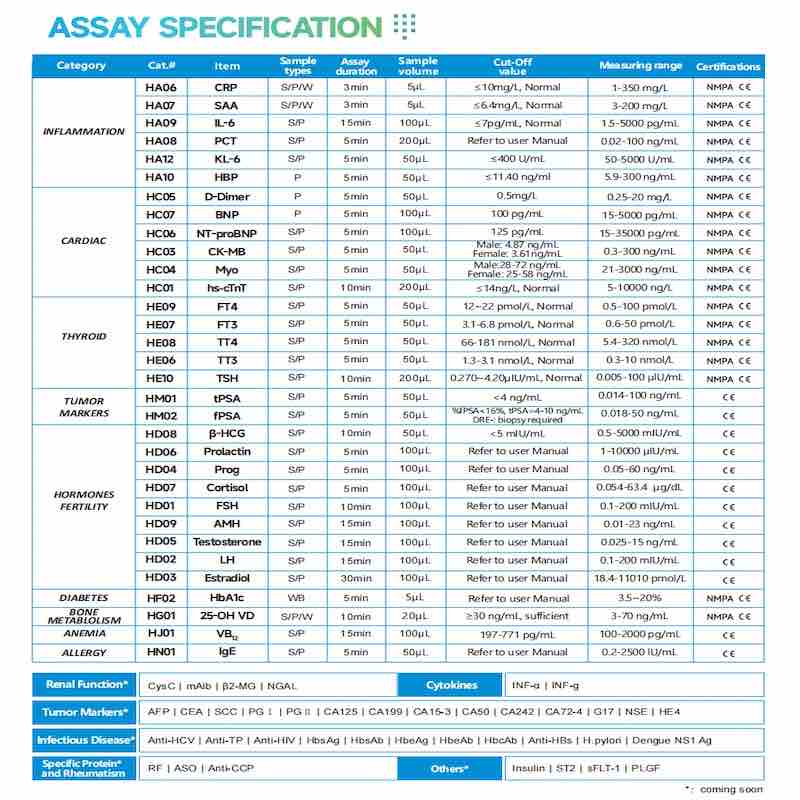
Poclight, en tant que fabricant, possède des brevets de recherche et développement indépendants. Et nos produits, y compris l'analyseur de clia sec poct du laboratoire de détection de cytokines , et les réactifs de détection —— Réactifs de laboratoire de détection de cytokines poct clia , peuvent vous apporter des tests rapides, précis et faciles. Si vous êtes intéressé par notre analyseur d'immunoessai portatif de micro-chimiluminescence Poct d'urgence clinique de laboratoire personnalisé OEM en Chine, n'hésitez pas à nous contacter et nous pouvons vous fournir un fournisseur de confiance de solutions de laboratoire et de poct .

 English
English français
français русский
русский español
español português
português العربية
العربية 日本語
日本語 Türkçe
Türkçe हिंदी
हिंदी Indonesia
Indonesia 








 Network IPv6 pris en charge |
Network IPv6 pris en charge | 